Como hemos visto anteriormente, los átomos son esas partículas diminutas, indivisibles e inalterables, de que están formados los elementos existentes en la naturaleza.
Los átomos tienen la tendencia a completar sus últimas órbitas con una cantidad de 8 electrones. Esta propiedad es conocida como la regla del octeto. En estos casos, los electrones de la última capa literalmente hacen una “valla” alrededor del átomo e impiden que cualquier fuerza externa que se llegue a presentar los desprenda de su órbita. Cuando algunos átomos se combinan comparten las órbitas externas dando lugar a una especie de órbita común; si esta órbita común adquiere la configuración de 8 electrones, las molécula resultantes reciben el nombre de aislantes.
Se han desarrollado muchos modelos de la estructura del átomo para poder estudiarlo, algunos muy simples, otros muy complejos. Como electricistas, no necesitamos conocer los modelos más complejos de la estructura del átomo para entender el comportamiento de la electricidad en las instalaciones eléctricas residenciales. Vamos a analizar el modelo propuesto en 1913 por el físico danés Niels Bohr, ya que es uno de los modelos más sencillos de entender, pues compara la estructura del átomo con la del sistema solar.
Según este modelo, los átomos tienen una forma similar a la del sistema solar, con unas partículas alojadas en un centro llamado Núcleo, y otras partículas girando en trayectorias cerradas alrededor del núcleo llamadas Órbitas.
El núcleo está formado por varías partículas, pero las que nos interesan reciben el nombre de protones, a las cuales se les ha asignado un valor positivo, también llamado carga positiva.
A diferencia del sistema solar, donde el sol, ubicado en el centro del sistema, es el astro más grande, las partículas en el núcleo del átomo son mucho más pequeñas que aquellas girando en las órbitas; sin embargo, estas partículas concentran la mayor parte del peso del átomo. Es decir, los protones son las partículas más pequeñas del átomo, pero también son las más pesadas. Podríamos compararlas con pequeñas canicas, con tanto peso que se pegan entre sí, como si estuvieran unidas con “Kola-loka”. Esto evita que se muevan, de hecho, los protones siempre permanecen en su sitio.
A diferencia del sistema solar, donde el sol, ubicado en el centro del sistema, es el astro más grande, las partículas en el núcleo del átomo son mucho más pequeñas que aquellas girando en las órbitas; sin embargo, estas partículas concentran la mayor parte del peso del átomo. Es decir, los protones son las partículas más pequeñas del átomo, pero también son las más pesadas. Podríamos compararlas con pequeñas canicas, con tanto peso que se pegan entre sí, como si estuvieran unidas con “Kola-loka”. Esto evita que se muevan, de hecho, los protones siempre permanecen en su sitio.
La cantidad de protones en el núcleo de un átomo recibe el nombre de número atómico. Este número le otorga a cada átomo su identidad química. Un átomo con un protón es un átomo de hidrógeno, uno con dos protones es helio, con tres protones litio y así sucesivamente siguiendo la escala. También define su ubicación en la llamada tabla periódica de los elementos. Por ejemplo, el cobre tiene 29 protones en el núcleo, y ocupa el lugar número 29 en la tabla periódica.
En las órbitas se encuentran las partículas llamadas electrones, a las cuales se les ha asignado el valor o carga negativa. A pesar de ser partículas relativamente grandes, comparadas con los protones, también son las más ligeras; podríamos compararlas con enormes burbujas de jabón, con tan poquito peso, que pueden girar fácilmente alrededor del núcleo.
Un átomo en su estado natural es neutro y tiene un número igual de electrones y protones. Sin embargo, cada órbita puede contener un cierto número máximo de electrones: la primera órbita puede contener hasta 2 electrones, la segunda hasta 8 electrones, la tercera puede tener hasta 18 electrones, la cuarta hasta 32 electrones, la quinta hasta 50 electrones, la sexta hasta 72 electrones y la séptima hasta 98 electrones.
Los átomos tienen la tendencia a completar sus últimas órbitas con una cantidad de 8 electrones. Esta propiedad es conocida como la regla del octeto. En estos casos, los electrones de la última capa literalmente hacen una “valla” alrededor del átomo e impiden que cualquier fuerza externa que se llegue a presentar los desprenda de su órbita. Cuando algunos átomos se combinan comparten las órbitas externas dando lugar a una especie de órbita común; si esta órbita común adquiere la configuración de 8 electrones, las molécula resultantes reciben el nombre de aislantes.
 |
| Átomo de neón, con diez protones en el núcleo y diez electrones en las órbitas. La última órbita contiene ocho electrones haciéndolo un elemento muy estable. |
Cuando existe un solo electrón en la última órbita, este puede desprenderse más fácilmente del átomo, por eso se le llama electrón libre. Si se manifiesta una fuerza que logre arrancar a los electrones libres de sus órbitas y hacer que se desplacen hacia otros átomos, entonces se produce la carga eléctrica de un cuerpo. Podemos decir que la electricidad está hecha de electrones libres. Los materiales que presentan electrones libres se llaman conductores.
Si queremos controlar a la electricidad, primero debemos poder medirla. Como la electricidad está hecha de electrones libres, la unidad elemental para medir carga eléctrica es el electrón libre. ¿Te imaginas cuantos electrones libres hay por ejemplo en un pedazo de alambre de cobre? Sería imposible de contar ya que el electrón libre es una es una unidad muy pequeña; sería casi como contar la cantidad de arena de una playa grano por grano. Sin embargo, cuando necesitamos contar cantidades de partículas pequeñas (por ejemplo el arroz, el frijol, el maíz o la arena misma) se utilizan "paquetes" (bolsas o cajas) que aunque se miden por volumen, suponemos que pueden contener aproximadamente la misma cantidad de partículas. Por ejemplo, se calcula que en una bolsa con un kilogramo de arroz hay aproximadamente unos 30000 granos. De forma similar, el el sistema internacional de unidades, para medir la carga eléctrica se utiliza una unidad llamada Coulomb (en honor al físico francés Charles Coulomb). Esta unidad equivale a tener agrupados unos 6 billones de billones de electrones libres.
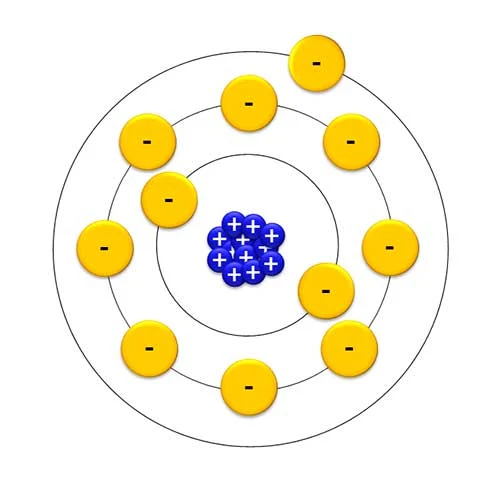 |
| Átomo de sodio, con electrón libre en la última órbita |
Si queremos controlar a la electricidad, primero debemos poder medirla. Como la electricidad está hecha de electrones libres, la unidad elemental para medir carga eléctrica es el electrón libre. ¿Te imaginas cuantos electrones libres hay por ejemplo en un pedazo de alambre de cobre? Sería imposible de contar ya que el electrón libre es una es una unidad muy pequeña; sería casi como contar la cantidad de arena de una playa grano por grano. Sin embargo, cuando necesitamos contar cantidades de partículas pequeñas (por ejemplo el arroz, el frijol, el maíz o la arena misma) se utilizan "paquetes" (bolsas o cajas) que aunque se miden por volumen, suponemos que pueden contener aproximadamente la misma cantidad de partículas. Por ejemplo, se calcula que en una bolsa con un kilogramo de arroz hay aproximadamente unos 30000 granos. De forma similar, el el sistema internacional de unidades, para medir la carga eléctrica se utiliza una unidad llamada Coulomb (en honor al físico francés Charles Coulomb). Esta unidad equivale a tener agrupados unos 6 billones de billones de electrones libres.



No hay comentarios.:
Publicar un comentario